Меню
 БИОРИТМ
ООО "МФК БИОРИТМ"
БИОРИТМ
ООО "МФК БИОРИТМ"
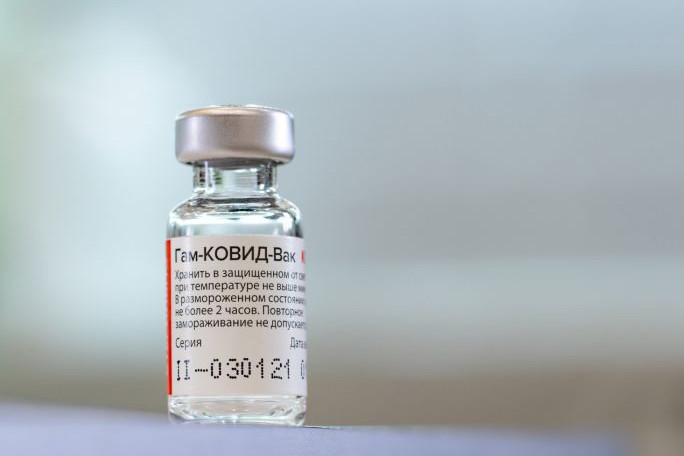
Центр им. Гамалеи получил регистрационное удостоверение на новую вакцину от COVID-19. Она предназначена для детей от 6 до 11 лет. В ней содержится 1/10 дозы «Спутника V», применяемого для взрослых.
 В реестре лекарственных средств появилась запись о регистрации вакцины для профилактики COVID-19 для детей от 6 до 11 лет. Вакцина называется «Гам-КОВИД-Вак-Д».
В реестре лекарственных средств появилась запись о регистрации вакцины для профилактики COVID-19 для детей от 6 до 11 лет. Вакцина называется «Гам-КОВИД-Вак-Д». Препарат, как и взрослый вариант, состоит из двух компонентов. В вакцине для детей содержится 1/10 взрослой дозы «Спутника V». Она выпускается в форме раствора для внутримышечного введения. Согласно ГРЛС, у препарата один производитель — филиал «Медгамал» Центра им. Н.Ф. Гамалеи. Заявление на регистрацию было подано в январе 2023 года. Регистрация действительна до 1 января 2024 года.
В России уже зарегистрирована вакцина для подростков от 12 до 17 лет «Спутник М» («Гам-КОВИД-Вак-М»). Она поступила в гражданский оборот.
Как сообщал «ФВ», заявку на исследование вакцины для детей от 6 до 11 лет Центр им. Н.Ф. Гамалеи подал в ноябре 2021 года. Глава центра Александр Гинцбург ожидал, что вакцину против коронавирусной инфекции для детей старше шести лет не нужно будет регистрировать отдельно. Вакцинацию детей данной возрастной категории планировалось начать в феврале 2022 года. Тогда же президент заявил о необходимости создать вакцину от коронавируса для детей старше двух лет.
В январе 2021 года премьер-министр подписал распоряжение, в соответствии с которым Центру им. Н.Ф. Гамалеи выделялось 305 млн руб. из резервного фонда правительства на проведение исследования вакцины «Гам-КОВИД-Вак-М» среди добровольцев 6—11 лет.
- Создано: 17.04.2023

MSD купит компанию Prometheus Biosciences. Сумма сделки составит 11 млрд долл., она позволит производителю усилить свои позиции в области иммунологии.
 SD (в США и Канаде — Merck&Co) купит Prometheus Biosciences за 10,8 млрд долл., об этом сообщается на сайте компании. Благодаря этой сделке американский производитель получит доступ к перспективному экспериментальному препарату от язвенного колита и болезни Крона и сможет расширить свои возможности в области иммунологии.
SD (в США и Канаде — Merck&Co) купит Prometheus Biosciences за 10,8 млрд долл., об этом сообщается на сайте компании. Благодаря этой сделке американский производитель получит доступ к перспективному экспериментальному препарату от язвенного колита и болезни Крона и сможет расширить свои возможности в области иммунологии.«Это позволит нам активно продвигаться в области иммунологии и, как мы думаем, обеспечит нам устойчивый рост вплоть до 2030-х годов, учитывая долгий срок действия патентов», — заявил генеральный директор MSD Роберт Дэвис.
По словам Дэвиса, препарат Prometheus под названием PRA023, который предназначен для лечения язвенного колита, болезни Крона и других аутоиммунных заболеваний, может принести MSD многомиллиардные продажи. Дэвис заявил: если сделка, как ожидается, будет закрыта в III квартале этого года, компания может запустить исследование препарата на поздних стадиях против язвенного колита в IV квартале этого или I квартале 2024 года.
Reuters пишет, что MSD концентрируется на сделках, чтобы справиться с потерей доходов, так как к концу десятилетия истекает срок действия патентов на иммунотерапию против рака «Китруда». Как раз к этому времени доход от препаратов, которые компания приобрела в рамках сделки с Prometheus, начнет поступать примерно в то время, заявил Дэвис.
Он сравнил эту сделку с приобретением Acceleron в 2021 году. «Я считаю, что теперь у нас очень сильный портфель в области кардиометаболических препаратов. Мы видим, что это приобретение Prometheus создаст аналогичный портфель в области иммунологии», — заявил он.
- Создано: 17.04.2023

Михаил Мишустин утвердил концепцию увеличения заготовки плазмы крови для производства лекарств на период до 2030 года. На ее реализацию в ближайшие три года направят почти 8 млрд рублей.
В рамках концепции планируется:
- модернизировать учреждения, которые занимаются сбором и хранением крови,
- снизить стоимость заготовки плазмы за счет увеличения объемов,
- развивать взаимодействие с донорами.
Концепцию реализуют в 3 этапа:
С 2023 по 2024 год пройдет модернизация плазмоцентров и учреждений Службы крови Федерального медико-биологического агентства (ФМБА). С 2025 по 2027 год региональные учреждения Службы крови будут переоснащены, а объем заготовки плазмы увеличат до 1,2 млн литров в год. С 2028 по 2030 год объем заготовки крови планируется довести до 1,8 млн литров в год. Это позволит создать значительный запас сырья для производства лекарств и откроет возможности для экспорта.
- Создано: 15.02.2023
Первая фаза клинического исследования вакцины для профилактики респираторно-синцитиальной вирусной инфекции (РСВИ) началась в НИИ гриппа им. А. А. Смородинцева. Об этом рассказали в пресс-службе Минздрава РФ.
В рамках исследований специалисты изучат безопасность и иммуногенность новой вакцины. В будущем вакцинация может снизить заболеваемость и риск развития тяжелых форм болезни у пожилых людей и пациентов с иммунодефицитом. Отметим, что в настоящее время сертифицированные противовирусные средства, препараты и вакцины для специфической профилактики РСВИ.
РСВИ считают одной из главных причин тяжелых инфекций у маленьких детей. У взрослых болезнь протекает как заболевание верхних дыхательных путей с температурой 37-38 градусов в виде ринита, фарингита и ларингита. Длится заболевание от пяти дней до трех недель.
Ранее «Ъ» рассказывал, что в России сокращаются клинические испытания оригинальных лекарств. В 2022 году Минздрав выдал на 18,5% меньше разрешений, чем годом ранее. Падение стало следствием массового отказа иностранных компаний от исследований в стране, хотя лекарства и медицинские изделия не попали под санкции.
- Создано: 15.02.2023

По данным Национальной системы цифровой маркировки товаров «Честный знак», сейчас полностью или более чем на 90% собственным производством обеспечивается почти половина всех лекарств из списка ЖНВЛП: 364 наименования из 821 в перечне. То есть как минимум 9 из 10 пачек каждого из этих лекарств производится в РФ. По 300 наименованиям Россия импортонезависима полностью. С начала года полностью импортозамещены 45 препаратов.
За 9 месяцев 2022 года в России выросло производство лекарственных препаратов на 5% к аналогичному периоду прошлого года, посчитали аналитики «Честного знака».
- Создано: 19.12.2022

Решение принято в связи с ростом случаев заболевания гриппом, в том числе в сочетании с коронавирусом.
Тестирование будет проводиться в рамках программы государственных гарантий бесплатного оказания гражданам медицинской помощи. Постановление о порядке проведения таких исследований подписал председатель Правительства Михаил Мишустин.
Решение принято в связи с ростом случаев заболевания гриппом, в том числе в сочетании с коронавирусом.
«В настоящее время мы наблюдаем подъем заболеваемости как новой коронавирусной инфекцией, так и гриппом. Поскольку тактика лечения COVID-19 и гриппа отличается, необходимо знать какой именно вирус вызвал заболевание, чтобы правильно оказать помощь и назначить лечение пациенту», — пояснил главный внештатный специалист Минздрава России по инфекционным болезням, профессор Владимир Чуланов.
Тестирование на грипп в рамках программы ОМС позволит:
- расширить доступность оказания медицинской помощи для граждан;
- своевременно поставить диагноз и снизить до минимума риски тяжелого течения заболевания и неблагоприятных исходов. Исследования на грипп и ОРВИ могут проводиться одновременно с ПЦР-тестом на коронавирус при наличии показаний.
Решение о необходимости тестирования на грипп конкретного пациента принимает врач.
Тестирование на грипп людей с симптомами острой респираторной вирусной инфекции поможет снизить риски для заболевших.
- Создано: 19.12.2022

В настоящее время в стране используется только одна тринадцативалентная вакцина от пневмококковой инфекции Превенар 13 производства Pfizer (США). Вторая тринадцативалентная вакцина Пнемотекс российского производителя ООО «Нанолек» будет выпущена на рынок после согласования ее стоимости. Это повысит ассортиментную доступность пневмококковых вакцин для граждан.
Согласованная цена на суспензию для внутримышечного введения составила 1380,57 рубля за одну дозу.
Полное торговое наименование вакцины — Пнемотекс (вакцина пневмококковая полисахаридная конъюгированная адсорбированная тринадцативалентная). Лекарственный препарат включен в перечень жизненно необходимых и важнейших (ЖНВЛП).
- Создано: 19.10.2022

Минздрав России одобрил включение в инструкцию по медицинскому применению ботулинического токсина типа А Релатокс® нового показания. Теперь препарат можно назначать при хронической мигрени у взрослых с 18 до 65 лет.
Препарат Релатокс® представляет собой первый российский ботулинический токсин, применяющийся в косметологии для коррекции мимических морщин и гипергидроза, а также в неврологической практике для лечения блефароспазма, спастичности мышц верхней конечности после перенесенного ишемического инсульта, спастичности верхней и нижней конечности у детей 2—17 лет с ДЦП и цервикальной дистонии у взрослых.
Механизм действия ботулинического токсина типа А при лечении хронической мигрени основан на блокировании нервно-мышечной передачи, позволяющем снижать тонус мышц головы и уменьшать раздражение нервных окончаний, а также на способности препарата ингибировать болевые медиаторы и подавлять нейрогенные воспаления в нервной системе, что приводит к снижению интенсивности боли, снижению частоты приступов мигрени или полному их исчезновению.
НПО «Микроген» (входит в холдинг «Нацимбио» Госкорпорации Ростех) успешно завершило проведение клинических исследований препарата Релатокс® на базе пяти независимых центров, расположенных в Москве, Красноярске и Санкт-Петербурге, для оценки его эффективности и безопасности в терапии хронической мигрени. В них приняли участие 220 пациентов в возрасте от 18 до 65 лет.
Согласно полученным результатам, применение препарата оказывало значимое положительное влияние на количественные характеристики заболевания, а также на качество жизни пациентов с хронической мигренью. Так, у пациентов с мигренью на 9 дней в месяц сократилась длительность приема препаратов против головной боли, а также снизились сопутствующие симптомы мигрени — тошнота, фото- и фонофобия.
- Создано: 19.10.2022

ООО «НПО Петровакс Фарм» (далее Компания или «Петровакс») объявляет об изменениях в составе участников. Президент компании «Петровакс» Михаил Цыферов и инвестиционная компания VB Partners выкупают 100% Компании у холдинга «Интеррос» за счет собственных и заемных средств от консорциума банков. Таким образом предыдущий владелец полностью выходит из бизнеса «Петровакса».
Структуру и сумму сделки стороны не раскрывают.
Михаил Цыферов возглавляет «Петровакс» с 2018 года. По итогам сделки Михаил полностью сосредоточится на управлении Компанией, покинув другие должности.
«Мы благодарны «Интерросу» за их экспертизу и вклад в развитие Компании, которая прошла существенную трансформацию и сумела занять новые ниши на фармацевтических рынках не только в России, но и за рубежом. Выкуп актива — это следующий логичный шаг в развитии: новая акционерная структура позволит Компании продолжать расти и обеспечит комфорт для всех стейкхолдеров», — заявил Михаил Цыферов, президент «Петровакс Фарм».
Участие в сделке инвестиционной компании VB Partners будет способствовать реализации потенциала «Петровакс». Стратегия компании направлена на создание и инвестирование в устойчивые бизнесы с понятной бизнес-моделью и эффективным менеджментом, что полностью отражает видение как команды «Петровакса», так и продающей стороны.
«Мы рады тому, что портфель наших активов пополнился компанией «Петровакс Фарм». Как сторонникам импакт-инвестиций для нас было логичным принять участие в этой сделке. Понятная стратегия компании, профессиональная команда руководителей, а также высокий потенциал российской фармацевтической отрасли позволят обеспечить рост и прибыльность «Петровакса» в среднесрочной перспективе», — заявил Михаил Бройтман, сооснователь инвесткомпании VB Partners.
- Создано: 03.10.2022

Представители фармотрасли не смогли добиться от правительства списка из 189 зарубежных лекарств от редких заболеваний, которые необходимо заменить отечественными аналогами. Это стало темой конференции «Что происходит на фармацевтическом рынке». Также участники обсудили ситуацию с поставками готовой продукции и сырья.
 В начале сентября зам. министра здравоохранения Сергей Глаголев рассказал, что Минздрав и Минпромторг составили перечень из 189 МНН, не имеющих аналогов в России, а Минпромторг распределит, кто из отечественных предприятий будет разрабатывать лекарства в оперативные сроки. Профессиональные объединения попытались узнать, какие препараты внесены в этот перечень.
В начале сентября зам. министра здравоохранения Сергей Глаголев рассказал, что Минздрав и Минпромторг составили перечень из 189 МНН, не имеющих аналогов в России, а Минпромторг распределит, кто из отечественных предприятий будет разрабатывать лекарства в оперативные сроки. Профессиональные объединения попытались узнать, какие препараты внесены в этот перечень.На запрос союза фармпроизводителей из Минпромторга пришел ответ, что с перечнем ознакомиться нельзя, так как это информация для служебного пользования, сообщила исполнительный директор СПФО Лилия Титова. Об этом она рассказала на международной конференции «Что происходит на фармацевтическом рынке», прошедшей в Москве 3 октября, передает корреспондент «ФВ».
О чем не знает фарма
Аналогичный ответ получил директор АРФП Виктор Дмитриев. «Мы обратились и в Минздрав, и в Минпром. В Минпроме нам ответили, чтобы мы обращались в Минздрав. В Минздраве предложили по вопросу критериев отбора компаний, которым может быть поручена реализация разработки отечественных аналогов зарубежных препаратов, обратиться в Минпромторг России. А информация о перечне лекарств по постановлению правительства № 1233* отнесена к информации служебной информации ограниченного распространения и не подлежит разглашению», – процитировал он ответ ведомства.
Председатель правления Ассоциации фармпроизводителей ЕАЭС Алексей Кедрин рассказал об еще одном не очень публичном проекте. Он поинтересовался у участников конференции, знают ли они подробности программы развития, которую правительство обсудило 31 августа 2022 года. Ответ был отрицательным. По словам Кедрина, на этой стратсессии правительство «финализировало видение того, как будут развиваться промышленность, включая фарму».
«То, что известно мне: там есть предложения по развитию производства фармсубстанций и создания стандартных образцов, остальное все очень абстрактно. Почему бы ассоциациям или отдельным компаниям не задаться вопросом, насколько то, что планируется до 2030 года, отвечает моему видению на бизнес, и предложить добавить то, что необходимо», – призвал он собравшихся.
Как работает фарма в условиях санкций
Что касается цен на сырье, то, по словам Валиева, весной из-за резких изменений курсов валют стоимость некоторого сырья выросла на 40%, но сейчас цены нормализовались, удалось заместить поставщиков сырья и вспомогательных веществ на производителей из Южной Азии и Индии. По сырью ситуация зависит только от обменного курса рубля к тем валютам, в которых покупается продукция. С упаковкой оказалось сложнее: цены на стекло, картон, пластик по-прежнему выше уровня 2021 года примерно на 25%.
В кулуарах производители говорили, что не удается решить проблему с хроматографическими колонками, стандартными образцами. Поставки этого товара до сих пор похожи на прохождение квеста. Также не облегчило отечественным производителям исключение фармпродукции из запрета на автомобильные грузоперевозки по территории России из недружественных стран. Часть продукции, необходимая для производства, не квалифицируется как фармпродукция.
Лилия Титова констатировала, что фарме не удалось переубедить Минфин в необходимости снизить пошлины на внесение изменений в регдосье.
Как отметил генеральный директор ЦВ «Протек» Дмитрий Погребинский, дефектура периодически возникает, но нельзя сказать, что все плохо. В июле — августе была напряженная ситуация с задолженностью аптек, сейчас она улучшается. «Та работа, которую мы проделали с другими дистрибьюторами и производителями с 2018 года, привела к тому, что наши партнеры стали более внимательно следить за своими финансами», – отметил он.
*Постановление Правительства РФ № 1233 от 03.11.1994 «Об утверждении Положения о порядке обращения со служебной информацией ограниченного распространения в федеральных органах исполнительной власти, уполномоченном органе управления использованием атомной энергии и уполномоченном органе по космической деятельности».
- Создано: 03.10.2022
Ещё статьи...
.